Энергия ионизации атома
Энергия ионизации — количество энергии, необходимое для отрыва электрона от невозбужденного атома.
Энергия ионизации атома выражается в килоджоулях на моль (кДж/моль); допускается внесистемная единица электрон-вольт (эВ) на атом.
Для многоэлектронных атомов рассматриваются разные энергии ионизации, которые соответствуют отрыву первого, второго и так далее электронов. Чем больше число оторванных электронов, тем выше положительный заряд иона, и тем труднее их отрывать, поэтому энергия ионизации для каждого последующего электрона в этом случае возрастает.
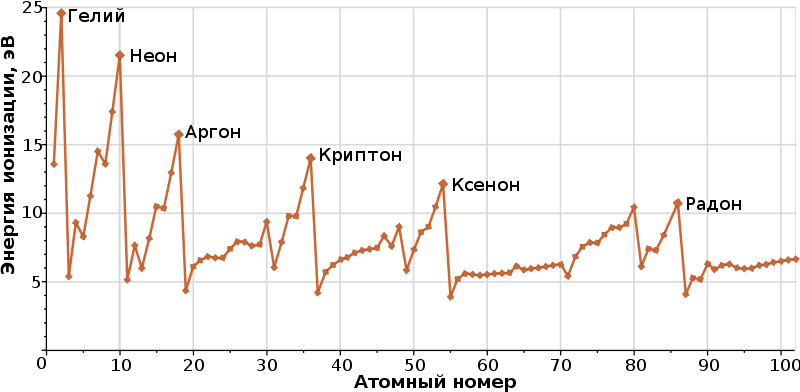
Энергия ионизации атома зависит от его электронной конфигурации. В частности, завершенные электронные слои обнаруживают повышенную устойчивость. Поскольку электронная конфигурация изменяется по периодическому закону Менделеева, энергия ионизации также следует ему (см. рисунок).
| Z | Элемент | I | II | III | |||
|---|---|---|---|---|---|---|---|
| I·10−2, кДж/моль | I, эВ на 1 атом | I·10−2, кДж/моль | I, эВ на 1 атом | I·10−2, кДж/моль | I, эВ на 1 атом | ||
| 1 | H | 13,12 | 13,60 | — | — | — | — |
| 2 | Не | 23,73 | 24,59 | 52,51 | 54,42 | — | — |
| 3 | Li | 5,20 | 5,39 | 72,99 | 75,64 | 117,70 | 122,00 |
| 5 | В | 8,01 | 8,30 | 24,27 | 25,16 | 36,70 | 38,00 |
| 6 | С | 10,86 | 13,26 | 23,53 | 24,38 | 46,30 | 48,00 |
| 7 | N | 14,02 | 14,53 | 28,57 | 29,60 | 45,30 | 47,00 |
| 8 | О | 13,14 | 13,62 | 33,89 | 35,12 | 53,10 | 55,00 |
| 9 | F | 16,81 | 17,42 | 33,76 | 34,98 | 60,80 | 63,00 |
| 11 | Na | 4,95 | 5,14 | 45,65 | 47,30 | 69,50 | 72,00 |
| 12 | Mg | 7,38 | 7,65 | 14,51 | 15,04 | 101,30 | 105,00 |
| 13 | Al | 5,78 | 5,99 | 18,17 | 18,83 | 27,00 | 28,00 |
| 14 | Si | 7,87 | 8,15 | 15,77 | 16,34 | 31,80 | 33,00 |
| 15 | P | 10,12 | 10,49 | 19,04 | 19,73 | 28,90 | 30,00 |
| 16 | S | 10,00 | 10,36 | 22,53 | 23,35 | 33,80 | 35,00 |
| 17 | Cl | 12,51 | 12,97 | 22,97 | 23,80 | 38,60 | 40,00 |
| 20 | Ca | 5,90 | 6,11 | 11,45 | 11,87 | 49,20 | 51,00 |
| 32 | Ge | 7,62 | 7,90 | 15,38 | 15,94 | 32,80 | 34,00 |
| 33 | As | 9,47 | 9,82 | 17,97 | 18,62 | 27,00 | 28,00 |
| 34 | Se | 9,41 | 9,75 | 20,45 | 21,19 | 32,80 | 34,00 |
| 35 | Br | 11,42 | 11,84 | 21,04 | 21,80 | 34,70 | 36,00 |
| 37 | Rb | 4,03 | 4,18 | 23,52 | 24,37 | 38,60 | 40,00 |
| 38 | Sr | 5,49 | 5,69 | 10,64 | 11,03 | 41,50 | 43,00 |
| 50 | Sn | 7,09 | 7,34 | 14,12 | 14,63 | 28,90 | 30,00 |
| 52 | Те | 8,69 | 9,01 | 17,95 | 18,60 | 28,90 | 30,00 |
| 53 | I | 10,08 | 10,45 | 18,43 | 19,10 | 29,90 | 31,00 |
| 56 | Ba | 5,03 | 5,21 | 96,54 | 10,00 | 35,70 | 37,00 |
| Элемент | I1 | I2 | I3 | I4 | I5 | I6 | I7 |
|---|---|---|---|---|---|---|---|
| Na | 495,8 | 4564 | — | — | — | — | — |
| Mg | 737,7 | 1451 | 7730 | — | — | — | — |
| Al | 577,6 | 1817 | 2744 | 11600 | — | — | — |
| Si | 786,5 | 1577 | 3228 | 4350 | 16100 | — | — |
| P | 1011,8 | 1904 | 2910 | 4950 | 6270 | 21200 | — |
| S | 999,6 | 2253 | 3380 | 4565 | 6950 | 8490 | 27000 |
| Cl | 1251,2 | 2296 | 3850 | 5160 | 6560 | 9360 | 11000 |
| Ar | 1520,6 | 2666 | 3946 | 5770 | 7230 | 8780 | 12000 |
Литература[править]
- Ахметов Н. С. Актуальные вопросы курса неорганической химии. — М.:Просвещение, 1991. — 224 с.